Проба Троммера
Это пример характерной реакции, которая в качестве «пробы» дает положительный или отрицательный результат — на основании наблюдений и сделанных из них выводов. Это один из способов определения преимущественно водорастворимых альдегидов и отличия их от кетонов — первое из этих соединений растворимо в воде, а второе — нет. Кроме того, проба Троммера подтверждает восстановительные свойства данных соединений. Альдегиды — это вещества, относящиеся к органическим соединениям. Для них характерно наличие альдегидной группы -СНО, связанной с атомом углерода в цепи. С другой стороны, кетоны содержат в своих молекулах кетогруппу, то есть атом углерода, связанный двойной связью с атомом кислорода (C=O).
Пробу Троммера проходят только альдегиды. Они также могут представлять собой восстанавливающие сахара (например, мальтозу или лактозу). В основном — это все соединения, которые могут окислять и в то же время восстанавливать ионы меди (II) (например, гидроксиламин, L-аскорбиновая кислота).
Интересно, что пробу Троммера изначально применяли не только для определения и изучения свойств альдегидов. Ее также использовали для определения сахара в моче.
Проведение пробы Троммера
Суть пробы Троммера заключается в добавлении к биологической жидкости 10 капель щелочи (10%), после чего в пробирку добавляется раствор сульфата меди (2,5%), пока в пробирке не образуется мутно-голубой раствор, содержащий следы оксида меди в виде нерастворенного осадка. Полученную жидкость нагревают горелкой, не доводя до кипения и не сбалтывая содержимое пробирки.
Если в биологической жидкости присутствует сахар, то из голубого цвета при нагревании жидкость превратится в смесь желтого цвета, образуя из окиси меди гидрат закиси меди.
Возможно также образование красного оттенка содержимого пробирки при образовании Cu2О, а при избыточном содержании в смеси сульфата меди цвет может быть изменен на черный.
При недостаточном количестве CuS04 в растворе возможно образование бурого цвета жидкости в пробирке.
УГЛЕВОДЫ
3.7.2. Свойства углеводов
Моносахариды и некоторые дисахариды, имеющие свободную альдегидную группу, обладают способностью восстанавливать в щелочной среде металлы из их оксидов в закисные формы или в свободное состояние (восстанавливающие сахара).
Опыт 4. Реакция Троммера
В щелочной среде глюкоза, являясь восстанавливающим сахаром, восстанавливает гидроксид меди (II) — Сu(ОН)2 до оксида меди (I) — Сu2О и при этом сама окисляется до глюконовой кислоты:

В одну пронумерованную пробирку вносят 10 капель 1 % раствора глюкозы, в другую — мальтозы, в третью — сахарозы, в четвертую — крахмала. В каждую пробирку добавляют по 10 капель 10 % раствора гидроксида натрия (NаОН) и по 2 капли 5 % раствора сульфата меди (II) — СUSO4, после чего нагревают. Наблюдают за выпадением кирпично-красного осадка в тех пробирках, которые содержат восстанавливающие сахара. В пробирках, содержащих невосстанавливающие сахара, образуется черный осадок.
В отчете требуется сделать вывод о том, какие углеводы являются восстанавливающими, а какие — нет.
Восстанавливающий сахар, окисляясь, восстанавливает висмут до закиси (гидратированной) или до свободного состояния.
Для приготовления реактива Ниландера в фарфоровой ступке смешивают 2 г нитрата висмута — Вi(NO3)3 и 4 г сегнетовой соли (К, Nа-виннокислый). Тщательно растирают и добавляют небольшими порциями 10 мл 10 % раствора гидроксида натрия (NаОН). Фильтруют, хранят в склянке темного стекла на холоде.
В четыре пронумерованные пробирки вносят по 10 капель раствора углевода (глюкозы, мальтозы, сахарозы и крахмала)
Добавляют в каждую пробирку 10 капель раствора Ниландера и осторожно кипятят в течение 2 минут. Наблюдают за появлением темно-коричневой окраски растворов с восстанавливающими сахарами
В отчете следует сделать вывод о том, какие углеводы являются восстанавливающими, а какие — нет.
Опыт 6. Реакция Селиванова на кетогексозы
Эта реакция позволяет различать альдозы (глюкоза) и кетозы (фруктоза). Для проведения опыта используют реактив Селиванова (резорцин, смешанный с несколькими каплями концентрированной соляной кислоты).
В две пробирки наливают по 2 мл реактива Селиванова. В одну из них добавляют 3 — 4 капли 2 % раствора фруктозы, а в другую — столько же 2 % раствора глюкозы. Обе пробирки нагревают на водяной бане (80 °С) 5 — 10 минут. Раствор с фруктозой окрашивается в оранжевый, а затем в розово-красный цвет. Раствор, содержащий глюкозу, не окрашивается. В отчете следует указать, почему.
В отчете результаты опытов оформляются в виде таблицы:
|
Название углевода |
Название реакции |
Наблюдаемые изменения |
Вывод |
Опыт 7. Кислотный гидролиз крахмала
В пробирку вносят 2 мл раствора крахмала, добавляют 4 мл воды и 10 капель концентрированной серной кислоты (Н2SO4). Пробирку помещают в кипящую водяную баню на 20 минут. При этом протекает гидролиз крахмала, и мутный раствор клейстера становится прозрачным.
Затем содержимое пробирки охлаждают и с полученным гидролизатом крахмала проводят еще две реакции.
Йодкрахмальная реакция. Наливают в чистую пробирку 1 мл полученного раствора (гидролизата) и добавляют 1 каплю раствора йода (см. опыт 3). Отмечают изменение окраски.
Если проба не дает положительной йодкрахмальной реакции, то 1 мл гидролизата отливают в другую пробирку и проводят реакцию Троммера.
Реакция Троммера. К предварительно отлитому 1 мл гидролизата добавляют 4 мл 10 % раствора гидроксида натрия (NаОН) для создания щелочной среды. После этого вносят 1 мл 5 % раствора сульфата меди (II) — СuSO4 и нагревают на кипящей водяной бане. Будет ли положительной проба Троммера? (См. опыт 4.) Наблюдается ли изменение окраски?
Сделать вывод о том, прошел или нет гидролиз крахмала. Что образовалось в результате гидролиза? Написать схему последовательного гидролиза крахмала.
ПредыдущаяСледующая
Применение пробы Троммера на практике
Проба Троммера представляет собой характерную реакцию, позволяющую качественно определять и изучать восстановительные свойства альдегидов, сахаров и других органических веществ.
Пробу Троммера проводят в несколько нижеследующих этапов.
- Первым этапом является осаждение свежего гидроксида меди (II). Данное соединение можно получить, например, в результате реакции гидроксида натрия (NaOH) с сульфатом меди (II) (CuSO4). Оба субстрата легко диссоциируют на ионы в водных растворах. Происходящая обменная реакция приводит к выпадению желеобразного осадка гидроксида меди (II) синего цвета (Cu(OH)2 нерастворим в воде). NaOH добавляют в избытке, чтобы обеспечить щелочную среду для пробы Троммера.
- Затем к приготовленному таким образом реагенту Троммера добавляют, например, альдегид (стоит придерживаться соотношения обоих реагентов 1:1). Применение избытка Cu(OH)2 приведет к ошибочным наблюдениям, так как образуется черный осадок CuO. Эту реакцию следует проводить на водяной бане, слегка нагревая смесь. Тогда происходящие процессы происходят быстрее.
- В результате реакции наблюдается изменение окраски с синей на кирпично-красную (положительный результат пробы Троммера). Это связано с продолжающейся окислительно-восстановительной реакцией. Альдегид, в частности его характерная альдегидная группа (-CHO), окисляется до карбоксильной группы (-COOH), которая присутствует в молекулах карбоновых кислот. С другой стороны, ионы меди (II) восстанавливаются до ионов меди (I) — кирпично-красного цвета.
- При наличии в пробирке соединений, не подвергающихся пробе Троммера, в результате нагревания смеси гидроксида меди (II) с испытываемым веществом образуется черный осадок. Это связано с разложением Cu(OH)2 на оксид меди (II) и воду.
Модификации пробы Троммера
Известны две модификации пробы Троммера: проба Фелинга и проба Бенедикта. На практике они оказались гораздо более эффективными и чувствительными по сравнению с первоначальным экспериментом. Поэтому пробу Троммера в настоящее время в лабораторной практике проводят редко. Все три метода исторически применяли главным образом для аналитического определения сахаров (глюкозы) в моче.
Проба Фелинга
Модификация пробы Фелинга заключается главным образом в том, что в качестве (слабого) окислителя не используется гидроксид меди (II). В этом случае применяют комплекс катионов меди вместе с тартратом калия-натрия (придает реагенту Фелинга синюю окраску). Благодаря этой процедуре данная реакция более эффективна, чем проба Троммера, поскольку комплекс тартрата и ионов меди (II) более растворим и, следовательно, более реакционноспособен. В случае положительного результата данной пробы также наблюдается образование осадка кирпично-красного цвета из Cu+.
Проба Бенедикта
Проба — троммер
Проба Троммера не является специфичной, а обусловлена наличием в глюкозе альдегидной группы.
Проба Троммера хороша тем, что может быть выполнена в самых примитивных условиях. В клинических лабораториях предпочитают пользоваться готовыми растворами комплексных соединений меди: реактивом Фелинга ( стр. Все эти реактивы не являются специфическими на глюкозу, и могут дать положительную пробу при наличии случайных веществ в моче. Так, например, положительная проба при отсутствии глюкозы в моче может получиться, если к моче для консервирования был добавлен формалин ( стр.
Положительна ли проба Троммера. Какие свойства гидролизата подтверждает эта реакция.
Как проводится проба Троммера на глюкозу. Какие свойства глюкозы открывают этой пробой.
Проверка производится пробами Троммера ( см. опыт 93, стр.
Записывают в таблицу результаты пробы Троммера и делают выводы.
Для обнаружения — сахара в моче пользуются пробами Троммера, Фелинга и Нилендера.
Простейшей клинической пробой на открытие глюкозы в моче является проба Троммера.
Этот же опыт показывает, что при консервировании мочи хлороформом клиническая проба Троммера на глюкозу ( стр.
Этот же опыт показывает, что при консервировании мочи хлороформом клиническая проба Троммера на глюкозу ( оп.
Пробирки выдерживают в термостате 15 мин при 38 С, затем выполняют пробу Троммера.
Реакция восстановления гидрата окиси меди в щелочной среде используется в клинических лабораториях под названием пробы Троммера, как простейшая реакция для открытия глюкозы в моче ( стр.
Наличие восстанавливающих свойств мочевой кислоты можег привести к частичному восстановлению гидрата окиси меди в моче при пробе Троммера на сахар, если производить ее неправильно, например допустить длительное кипячение. В связи с этим уже подчеркивалось ( см. опыт 63), что нагревать исследуемый раствор нужно только до кипения, В этих условиях глюкоза дает восстановление, а мочевая кислота не дает его.
Наличие восстанавливающих свойств мочевой кислоты может привести к частичному восстановлению гидроксида меди ( II) при пробе Троммера на сахар в моче, если проводить ее неправильно, например допустить длительное кипячение.
Наличие восстанавливающих свойств мочевой кислоты может привести к частичному восстановлению гидрата окиси меди в моче при пробе Троммера на сахар, если производить ее неправильно, например допустить длительное кипячение. В связи с этим уже подчеркивалось ( см. опыт 62), что нагревать исследуемый раствор нужно только до кипения. В этих условиях глюкоза дает восстановление, а мочевая кислота не дает его.
Химические свойства
Мальтоза – это альдегидо-спирто-гликозид.
I. Реакции открытой формы по — группе. Мальтоза дает все реакции по альдегидной группе с HCN, NH2OH, NH2–NH2, восстановления, окисления.
Проба Троммера и реакция Толленса положительны:
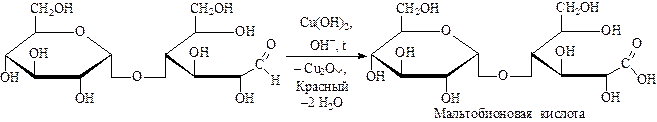
Углеводы, дающие положительную пробу Троммера, называются восстанавливающими.
II. Реакции по – ОН гр. аналогичны реакциям для сахарозы.
III. Мальтоза гидролизуется в кислой среде с образованием 2-х молекул глюкозы.
|
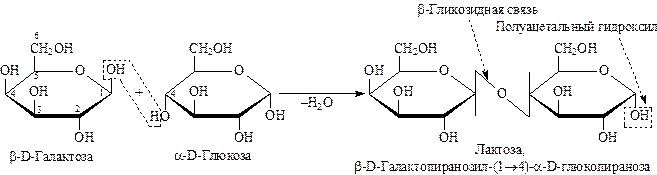
Лактоза существует в растворе в виде трех форм : двух циклических и одной открытой. Лактоза восстанавливающий дисахарид и обладает всеми свойствами, характерными для мальтозы. Лактоза содержится в женском молоке и способна подавлять рост бактерий.
Полисахариды
Это высокомолекулярные углеводы, содержащие сотни и даже тысячи моносахаридных остатков.
Из полисахаридов широко известны целлюлоза, крахмал и гликоген. Они построены из одного и того же моносахарида – D-глюкозы. Общая формула (С6Н10О5)n.
Целлюлоза (клетчатка) – самый распространенный не только полисахарид, но и органическое вещество в природе. Древесина примерно на 50% состоит из целлюлозы, а хлопок и лен представляют практически чистую целлюлозу.
В целлюлозе остатки D–глюкопиранозы связаны между собой b–(14) – гликозидной связью:
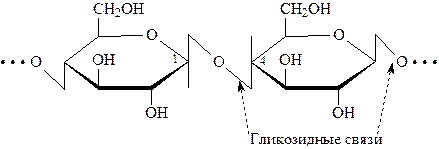
Цепь, построенная из тысячи остатков D–глюкозы, имеет линейное строение. Линейные цепи закреплены Н–связями между моносахаридными звеньями внутри одной цепи. Между параллельно уложенными цепями полисахарида также возникают Н-связи, придающие жесткость всей структуре. Отсюда высокая механическая прочность целлюлозы.
С химической позиции целлюлоза – многоатомный спирт, содержащий три гидроксильные группы в каждом моносахаридном звене, и способный образовывать с участием этих групп простые и сложные эфиры:
В эфирные группы могут быть превращены либо все, либо часть гидроксильных групп фрагмента полисахарида, где R–алкил или остаток органической или неоранической кислоты (в сложных эфирах). Целлюлоза не проявляет восстанавливающих свойств.
Простые эфиры целлюлозы – метилцеллюлоза R=CH3 и натрийкарбоксиметилцеллюлоза R=СН2 СООNa – образуют вязкие водные р-ры или гели и применяются в фармации в качестве загустителей, эмульгаторов и стабилизаторов мазей и эмульсий. Карбоксиметилцеллюлоза R=СН2СООН и диэтиламиноэтилцеллюлоза (сокращенно ДЭАЭ-целлюлоза) R=СН2СН2N (C2H5)2 обладают способностью ионитов и применяются в биохимических исследованиях.
Эфир уксусной к-ты (триацетат) применяют в производстве кинопленки и электроизоляционной пленки. Из этого полиэфира вырабатывают также ацетатное волокно. Из целлюлозы получают и другие искусственные волокна : вискозное и медноаммиачное.
Широко применяются эфиры целлюлозы с азотной к-той. Тринитрат целлюлозы – взрывчатое вещество, применяется в производстве пороха. Смесь моно-и динитратов целлюлозы используют в производстве целлулоида, лаков, взрывчатых вещ-в.
Гидролизом целлюлозы в промышленности вырабатывают глюкозу, брожением которой получают этиловый спирт. Другие области применения целлюлозы: строительный материал, производство бумаги, картона.
Крахмал – другой распространенный растительный полисахарид, состоящий из двух фракций: амилопектина (основной компонент – 80-90%) и амилозы. Амилоза, как и целлюлоза, построена из (14) – связанных остатков D–глюкопиранозы.
Однако в отличие от целлюлозы, гликозидная связь в амилозе имеет a-конфигурацию, в результате чего полисахаридная цепь приобретает иное пространственное строение, напоминающее спираль.
Амилоза + I2 синее окрашивание




























