Содержание:
Ключевое различие между молекулярным уравнением и ионным уравнением заключается в том, что молекулярное уравнение показывает реагенты и продукты в молекулярной форме, в то время как ионное уравнение показывает ионные частицы, участвующие в реакции.
Химические реакции — это взаимодействия между химическими соединениями с образованием новых соединений или перестройкой их химической структуры. Соединения, которые подвергаются определенной химической реакции, называются реагентами, а то, что мы получаем в конце, называется продуктом. Существуют различные формы химических уравнений, такие как молекулярные уравнения и ионные уравнения. В этой статье давайте рассмотрим разницу между молекулярным уравнением и ионным уравнением.
1. Обзор и основные отличия 2. Что такое молекулярное уравнение 3. Что такое ионное уравнение 4. Параллельное сравнение — молекулярное уравнение и ионное уравнение в табличной форме 5. Резюме
Электролитическая диссоциация
Электролитической диссоциацией называют процесс, в ходе которого молекулы растворенного вещества распадаются на ионы в результате взаимодействия с растворителем (воды). Диссоциация является обратимым процессом.
Диссоциация обуславливает ионную проводимость растворов электролитов. Чем больше молекул вещества распадается на ионы, тем лучше оно проводит электрический ток и является более сильным электролитом.
В общем виде процесс электролитической диссоциации можно представить так:
KA ⇄ K + (катион) + A — (анион)

Замечу, что сила кислоты определяется способностью отщеплять протон. Чем легче кислота его отщепляет, тем она сильнее.
У HF крайне затруднен процесс диссоциации из-за образования водородных связей между F (самым электроотрицательным элементом) одной молекулы и H другой молекулы.
Ступени диссоциации
Некоторые вещества диссоциируют на ионы не в одну стадию (как NaCl), а ступенчато. Это характерно для многоосновных кислот: H2SO4, H3PO4.
Посмотрите на ступенчатую диссоциацию ортофосфорной кислоты:
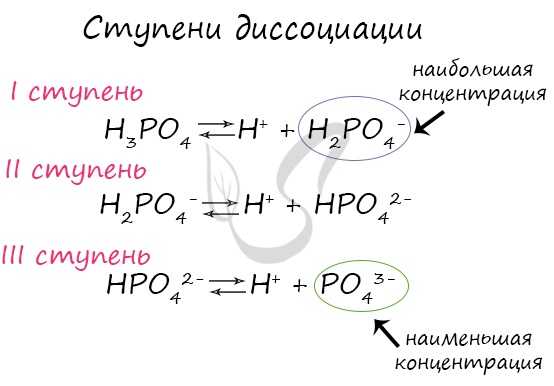
Важно заметить, что концентрация ионов на разных ступенях разная. На первых ступенях ионов всегда много, а до последних доходят не все молекулы
Поэтому в растворе ортофосфорной кислоты концентрация дигидрофосфат-анионов будет больше, чем фосфат-анионов.
Для серной кислоты диссоциация будет выглядеть так:
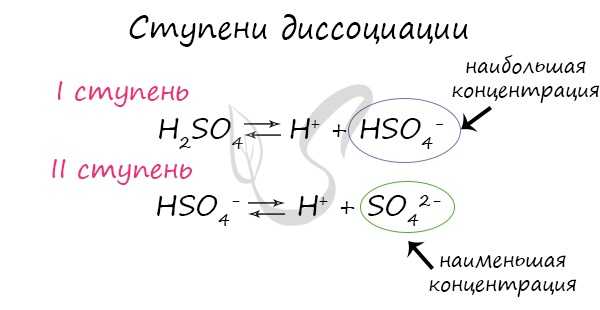
Для средних солей диссоциация чаще всего происходит в одну ступень:
Из одной молекулы ортофосфата натрия образовалось 4 иона.
Из одной молекулы сульфата калия образовалось 3 иона.
Электролиты и неэлектролиты
Химические вещества отличаются друг от друга по способности проводить электрический ток. Исходя из этой способности, вещества делятся на электролиты и неэлектролиты.
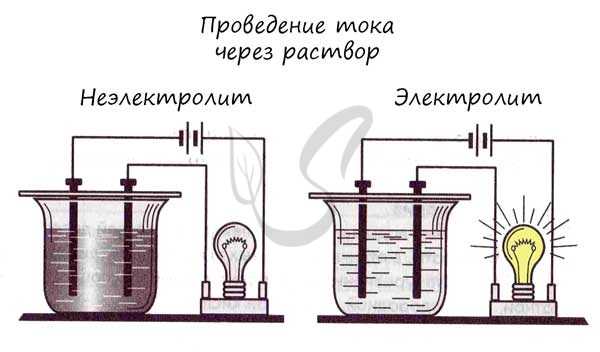
Электролиты — жидкие или твердые вещества, в которых присутствуют ионы, способные перемещаться и проводить электрический ток. Связи в их молекулах обычно ионные или ковалентные сильнополярные.
К ним относятся соли, сильные кислоты и щелочи (растворимые основания).
Степень диссоциации сильных электролитов составляет от 0,3 до 1, что означает 30-100% распад молекул, попавших в раствор, на ионы.

Неэлектролиты — вещества недиссоциирующие в растворах на ионы. В молекулах эти веществ связи ковалентные неполярные или слабополярные.
К неэлектролитам относятся многие органические вещества, слабые кислоты, нерастворимые в воде основания и гидроксид аммония.
Степень их диссоциации до 0 до 0.3, то есть в растворе неэлектролита на ионы распадается до 30% молекул. Они плохо или вообще не проводят электрический ток.
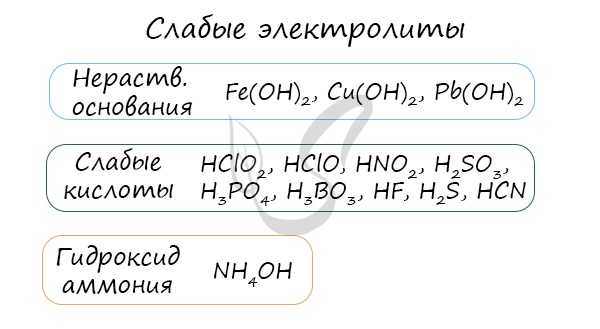
Молекулярное, полное и сокращенное ионные уравнения
Молекулярное уравнение представляет собой запись реакции с использованием молекул. Это те уравнения, к которым мы привыкли и которыми наиболее часто пользуемся. Примеры молекулярных уравнений:

Полные ионные уравнения записываются путем разложения молекул на ионы. Запомните, что нельзя раскладывать на ионы:
- Слабые электролиты (в их числе вода)
- Осадки
- Газы

Сокращенное ионное уравнение записывается путем сокращения одинаковых ионов из левой и правой части. Просто, как в математике — остается только то, что сократить нельзя.
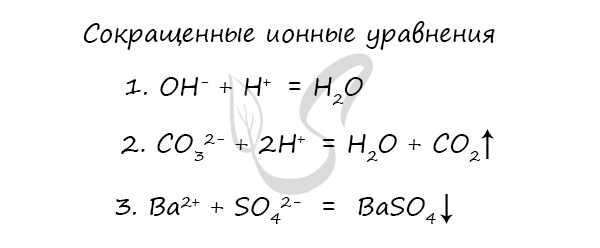
Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Электролитическая диссоциация
Похожие вопросы
- Все категории
- экономические 43,414
- гуманитарные 33,633
- юридические 17,906
- школьный раздел 608,054
- разное 16,856
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Чем отличаются молекулярные и ионные уравнения
Ключевое различие между молекулярным уравнением и ионным уравнением состоит в том, что молекулярное уравнение показывает реагенты и продукты в молекулярной форме, в то время как ионное уравнение показывает ионные частицы, участвующие в реакции.
Химические реакции — это взаимодействия между химическими соединениями с образованием новых соединений или перестройкой их химической структуры. Соединения, которые подвергаются определенной химической реакции, называют реагентом, а то, что мы получаем в конце, называют продуктом. Существуют различные формы химических уравнений, такие как молекулярные уравнения и ионные уравнения. В этой статье давайте рассмотрим разницу между молекулярным уравнением и ионным уравнением.
1. Обзор и основные отличия 2. Что такое молекулярное уравнение 3. Что такое ионное уравнение 4. Сравнение бок о бок — молекулярное уравнение и ионное уравнение в табличной форме 5. Резюме
Что такое молекулярное уравнение?
Молекулярное уравнение представляет реагенты и продукты в молекулярной форме. Напротив, ионное уравнение дает только ионные частицы, участвующие в химической реакции. Поэтому в молекулярном уравнении мы не должны включать никаких ионных частиц, только молекулы. Например, реакция между хлоридом натрия и нитратом серебра дает белый осадок, известный как хлорид серебра. Молекулярное уравнение для этой реакции выглядит следующим образом:
NaCl + AgNO3 ⟶ AgCl + NaNO3
Что такое ионное уравнение?
Ионное уравнение — это способ написания химического уравнения с использованием ионных частиц, которые были вовлечены в химическую реакцию. Существует два типа ионных уравнений: полное ионное уравнение и чистое ионное уравнение. Полное ионное уравнение — это химическое уравнение, которое объясняет химическую реакцию, четко указывая на ионные частицы, присутствующие в растворе. Ионный вид — это либо анион (отрицательно заряженный вид), либо катион (положительно заряженный вид). Напротив, полное молекулярное уравнение дает молекулы, которые принимают участие в химической реакции.

Чистое ионное уравнение представляет собой химическое уравнение, которое показывает ионы, которые участвовали в образовании конечного продукта. Кроме того, это уравнение может быть получено из полного ионного уравнения путем исключения аналогичных ионов с двух сторон полного ионного уравнения. Следовательно, чистое ионное уравнение не дает подробных сведений обо всех ионных компонентах, присутствующих в реакционной смеси. Для той же реакции, приведенной выше, ионное уравнение имеет следующий вид:
Na + + Cl– + Ag + + NO3– ⟶ AgCl + Na + + NO3–
В чем разница между молекулярным уравнением и ионным уравнением?
Молекулярное уравнение и ионное уравнение — это два типа химических уравнений, которые мы можем использовать для представления химических реакций. Ключевое различие между молекулярным уравнением и ионным уравнением состоит в том, что молекулярное уравнение показывает реагенты и продукты в молекулярной форме, в то время как ионное уравнение показывает только ионные частицы. Таким образом, молекулярное уравнение дается в молекулярной форме, тогда как ионное уравнение дается в ионной форме. Например, давайте посмотрим на реакцию между хлоридом натрия и нитратом серебра, которая дает белый осадок, известный как хлорид серебра. Его молекулярное уравнение NaCl + AgNO3 ⟶ AgCl + NaNO3, а ионное уравнение Na + + Cl– + Ag + + NO3– ⟶ AgCl + Na + + NO3–.
Ниже инфографики суммируется разница между молекулярным уравнением и ионным уравнением.

Резюме — Молекулярное уравнение против ионного уравнения
Молекулярное уравнение и ионное уравнение — это два типа химических уравнений, которые мы можем использовать для представления химических реакций. Как следует из их названий, молекулярное уравнение дается в молекулярной форме, тогда как ионное уравнение дается в ионной форме. Итак, ключевое различие между молекулярным уравнением и ионным уравнением заключается в том, что молекулярное уравнение показывает реагенты и продукты в молекулярной форме, в то время как ионное уравнение показывает только ионные частицы в реакции.
Ссылка:
1. Хельменстин, Энн Мари. «Определение молекулярного уравнения (химия)». ThoughtCo, 3 июля 2019 г., доступно здесь. 2. Хельменстин, Энн Мари. «Что такое ионное уравнение и как оно используется?» ThoughtCo, 1 августа 2019 г., доступно здесь.
Химия, Биология, подготовка к ГИА и ЕГЭ
Давайте разберем основные ионные химические реакции неорганической и некоторые реакции органической химии.
Очень часто в различных заданиях по химии просят написать не только химические уравнения в молекулярной форме, но и в ионной (полные и сокращенные). Как уже было замечено, ионные химические реакции идут в растворах. Зачастую, вещества распадаются на ионы именно в воде.
Полное ионное уравнение химической реакции: все соединения — электролиты, переписываем в ионном виде с учетом коэффициентов:
2Na + +2OH — +2H + + SO -2 = 2Na + + SO4 -2 + 2H2O — полное ионное уравнение реакции
Сокращенное ионное уравнение химической реакции: сокращаем одинаковые составляющие:
OH — + H + = H2O — сокращенное ионное уравнение реакции
По результатам этого сокращения одинаковых ионов видно, какие ионы образовали то, что нерастворимо или малорастворимо — газообразные продукты или реагенты, осадки или малодиссоциирующие вещества.
Не раскладывают на ионы в ионных химических реакциях вещества:
1. нерастворимые в воде соединения (или малорастворимые) (см. ТАБЛИЦЫ );
Сa 2+ + 2NO3 — + 2Na + +2OH — = Ca(OH)2 + 2Na + +2NO3 — — полное ионное уравнение реакции
Сa 2+ + 2OH — = Ca(OH)2 — сокращенное ионное уравнение реакции
2. газообразные вещества, например, O2, Cl2, NO и т.д.:
2Na + + S -2 + 2H + +2Cl — = 2Na + + 2Cl — + H2S — полное ионное уравнение реакции
S -2 + 2H + = H2S — сокращенное ионное уравнение реакции
3. малодиссоциирующие вещества (H2O, NH4OH);
OH — + H + = H2O — сокращенное ионное уравнение реакции
4. оксиды (все: и образованные металлами, и неметаллами);
2Ag + + 2NO3 — + 2Na + + 2OH — = Ag2O + 2NO3 — + 2Na + + H2O — полное ионное уравнение реакции
2Ag + + 2OH — = Ag2O + H2O — сокращенное ионное уравнение реакции
5. органические вещества (органические кислоты относят к малодиссоциирующим веществам)
CH3COOH + Na + + OH — = CH3COO — + Na + + H2O — полное ионное уравнение реакции
CH3COOH + OH — = CH3COO — + H2O — сокращенное ионное уравнение реакции
Зачастую ионные химические реакции — это реакции обмена .
Отличительной особенностью химических реакций ионного обмена от окислительно-восстановительных реакций является то, что они протекают без изменения степеней окисления, участвующих в реакции частиц.
- в ЕГЭ это вопрос А23 — Реакции ионного обмена
- в ГИА (ОГЭ) это А8— Реакции ионного обмена
Как составлять ионные уравнения. Задача 31 на ЕГЭ по химии
Достаточно часто школьникам и студентам приходится составлять т. н. ионные уравнения реакций. В частности, именно этой теме посвящена задача 31, предлагаемая на ЕГЭ по химии. В данной статье мы подробно обсудим алгоритм написания кратких и полных ионных уравнений, разберем много примеров разного уровня сложности.
Электролиты
При растворении в воде некоторые вещества имеют способность проводить электрический ток.
Электролиты проводят ток за счет так называемой ионной проводимости, которой обладают многие соединения с ионным строением (соли, кислоты, основания).
Вещества, имеющие сильнополярные связи, но в растворе при этом подвергаются неполной ионизации (например, хлорид ртути II) являются слабыми электролитами.
Многие органические соединения (углеводы, спирты), растворенные воде, не распадаются на ионы, а сохраняют свое молекулярное строение. Такие вещества электрический ток не проводят и называются неэлектролитами.
Приведем некоторые закономерности, руководствуясь которыми можно определить относятся вещества к сильным или слабым электролитам:
- Кислоты. К сильным кислотам из наиболее распространенных относятся HCl, HBr, HI, HNO3, H2SO4, HClO4. Все они являются сильными электролитами. Почти все остальные кислоты, в том числе и органические являются слабыми электролитами.
- Основания. Наиболее распространенные сильные основания – гидроксиды щелочных и щелочноземельных металлов (исключая Be) относятся к сильным электролитам. Слабый электролит – NH3.
- Соли. Большинство распространенных солей – ионных соединений — сильные электролиты. Исключения составляют, в основном, соли тяжелых металлов.
Теоретическая часть
Электролитической диссоциацией называется частичный или полный распад молекул электролита на ионы под действием полярных молекул растворителей.
Диссоциация протекает в результате сложного физико-химического взаимодействия молекул электролита с полярными молекулами растворителей. Взаимодействие ионов с полярными молекулами растворителя называется сольватацией (для водных растворов –гидратацией) ионов. В растворах электролитов образуются сольватированные ионы.
Электролиты проводят электрический ток в растворенном или расплавленном состоянии , так как в растворах имеются заряженные частицы: катионы и анионы.
Вещества, которые в растворенном или расплавленном состоянии не проводят электрического тока, называются неэлектролитами . Количественно процесс диссоциации характеризуется степенью электролитической диссоциации. Степенью диссоциации называется отношение числа молекул, распавшихся на ионы n к общему числу молекул N растворенного вещества:
· 100%
Степень диссоциации выражается в процентах или долях единицы. Электролиты делятся на три группы: а) сильные, б) средние, в) слабые.
Кислотами с точки зрения электролитической диссоциации называются электролиты, образующие в водных растворах положительно заряженные ионы водорода и анионы кислотного остатка.
Ионы водорода являются характерными для кислот и определяют их свойства. Кислоты, являющиеся сильными электролитами : азотная HNO 3 , соляная HCl, бромоводородная HBr, иодоводородная HJ, серная H 2 SO 4 ,марганцовая HMnO 4 и другие.
Слабых электролитов значительно больше, чем сильных. Слабыми электролитами являются кислоты: сернистая H 2 SO 3 , фтороводородная HF, угольная H 2 CO 3 , сероводородная H 2 S, уксусная CH 3 COOH и др.
Степень электролитической диссоциации
Дистанционные курсы для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Количество бюджетных мест в вузах по IT-программам вырастет до 160 тыс.
Время чтения: 2 минуты
Инфоурок стал резидентом Сколково
Время чтения: 2 минуты
Минобрнауки создаст для вузов рекомендации по поддержке молодых семей
Время чтения: 1 минута
Профессия педагога на третьем месте по популярности среди абитуриентов
Время чтения: 1 минута
В Забайкалье в 2022 году обеспечат интернетом 83 школы
Время чтения: 1 минута
Приемная кампания в вузах начнется 20 июня
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Как превратить молекулярное уравнение в полное ионное уравнение
Начинается самое интересное. Мы должны понять, какие вещества следует записывать в виде ионов, а какие — оставить в «молекулярной форме». Придется запомнить следующее.
В виде ионов записывают:
- растворимые соли (подчеркиваю, только соли хорошо растворимые в воде);
- щелочи (напомню, что щелочами называют растворимые в воде основания, но не NH 4 OH);
- сильные кислоты (H 2 SO 4 , HNO 3 , HCl, HBr, HI, HClO 4 , HClO 3 , H 2 SeO 4 , . ).
Как видите, запомнить этот список совсем несложно: в него входят сильные кислоты и основания и все растворимые соли. Кстати, особо бдительным юным химикам, которых может возмутить тот факт, что сильные электролиты (нерастворимые соли) не вошли в этот перечень, могу сообщить следующее: НЕвключение нерастворимых солей в данный список вовсе не отвергает того, что они являются сильными электролитами.
Все остальные вещества должны присутствовать в ионных уравнениях в виде молекул. Тем требовательным читателям, которых не устраивает расплывчатый термин «все остальные вещества», и которые, следуя примеру героя известного фильма, требуют «огласить полный список» даю следующую информацию.
В виде молекул записывают:
- все нерастворимые соли;
- все слабые основания (включая нерастворимые гидроксиды, NH 4 OH и сходные с ним вещества);
- все слабые кислоты (H 2 СO 3 , HNO 2 , H 2 S, H 2 SiO 3 , HCN, HClO, практически все органические кислоты . );
- вообще, все слабые электролиты (включая воду. );
- оксиды (всех типов);
- все газообразные соединения (в частности, H 2 , CO 2 , SO 2 , H 2 S, CO);
- простые вещества (металлы и неметаллы);
- практически все органические соединения (исключение — растворимые в воде соли органических кислот).
Уф-ф, кажется, я ничего не забыл! Хотя проще, по-моему, все же запомнить список N 1
Из принципиально важного в списке N 2 еще раз отмечу воду
Пример 2 . Составьте полное ионное уравнение, описывающие взаимодействие гидроксида меди (II) и соляной кислоты.
Решение . Начнем, естественно, с молекулярного уравнения. Гидроксид меди (II) — нерастворимое основание. Все нерастворимые основания реагируют с сильными кислотами с образованием соли и воды:
Cu(OH) 2 + 2HCl = CuCl 2 + 2H 2 O.
А теперь выясняем, какие вещества записывать в виде ионов, а какие — в виде молекул. Нам помогут приведенные выше списки. Гидроксид меди (II) — нерастворимое основание (см. таблицу растворимости), слабый электролит. Нерастворимые основания записывают в молекулярной форме. HCl — сильная кислота, в растворе практически полностью диссоциирует на ионы. CuCl 2 — растворимая соль. Записываем в ионной форме. Вода — только в виде молекул! Получаем полное ионное уравнение:
Сu(OH) 2 + 2H + + 2Cl — = Cu 2+ + 2Cl — + 2H 2 O.
Пример 3 . Составьте полное ионное уравнение реакции диоксида углерода с водным раствором NaOH.
Решение . Диоксид углерода — типичный кислотный оксид, NaOH — щелочь. При взаимодействии кислотных оксидов с водными растворами щелочей образуются соль и вода. Составляем молекулярное уравнение реакции (не забывайте, кстати, о коэффициентах):
CO 2 + 2NaOH = Na 2 CO 3 + H 2 O.
CO 2 — оксид, газообразное соединение; сохраняем молекулярную форму. NaOH — сильное основание (щелочь); записываем в виде ионов. Na 2 CO 3 — растворимая соль; пишем в виде ионов. Вода — слабый электролит, практически не диссоциирует; оставляем в молекулярной форме. Получаем следующее:
СO 2 + 2Na + + 2OH — = Na 2+ + CO 3 2- + H 2 O.
Пример 4 . Сульфид натрия в водном растворе реагирует с хлоридом цинка с образованием осадка. Составьте полное ионное уравнение данной реакции.
Решение . Сульфид натрия и хлорид цинка — это соли. При взаимодействии этих солей выпадает осадок сульфида цинка:
Na 2 S + ZnCl 2 = ZnS↓ + 2NaCl.
Я сразу запишу полное ионное уравнение, а вы самостоятельно проанализируете его:
2Na + + S 2- + Zn 2+ + 2Cl — = ZnS↓ + 2Na + + 2Cl — .
Предлагаю вам несколько заданий для самостоятельной работы и небольшой тест.
Упражнение 4 . Составьте молекулярные и полные ионные уравнения следующих реакций:
- NaOH + HNO 3 =
- H 2 SO 4 + MgO =
- Ca(NO 3 ) 2 + Na 3 PO 4 =
- CoBr 2 + Ca(OH) 2 =
Упражнение 5 . Напишите полные ионные уравнения, описывающие взаимодействие: а) оксида азота (V) с водным раствором гидроксида бария, б) раствора гидроксида цезия с иодоводородной кислотой, в) водных растворов сульфата меди и сульфида калия, г) гидроксида кальция и водного раствора нитрата железа (III).
В следующей части статьи мы научимся составлять краткие ионные уравнения и разберем большое количество примеров. Кроме того, мы обсудим специфические особенности задания 31, которое вам предстоит решать на ЕГЭ по химии.
Химия — это просто
- Популярно о химии
-
· Что такое химия
· Периодическая таблица - ОБЩАЯ ХИМИЯ
- Вещества и смеси
-
· Понятие вещества
· Вещество и его состояния
· Простые и сложные вещества
· Чистые вещества и смеси
· Свойства вещества
· Энергия вещества
· Газы
· Растворы
· Коллоидные растворы
· Состав растворов
· Электролитическая диссоциация
· Уравнение ионных реакций
· Степень диссоциации
· Диссоциация кислот и оснований
· Диссоциация воды
· Твердые вещества
· Неорганические вещества
· Оксиды
· Основания
· Кислоты
· Соли
· Гидролиз солей
· Электролиз - Атомы и молекулы
- Строение веществ
- Взаимодействие веществ
- НЕОРГАНИЧЕСКАЯ ХИМИЯ
- ОРГАНИЧЕСКАЯ ХИМИЯ
Ионно-молекулярные уравнения реакции
По этой ссылке вы найдёте полный курс лекций по математике:
Теория электролитической диссоциации признает, что все реакции в водных растворах электролитов являются реакциями между ионами. Поэтому уравнения реакции для этих процессов, записанные в молекулярной форме, не отражают истинного состояния веществ в растворах. Кроме записи уравнений реакций, в молекулярном виде существует ионная (ионно-молекулярная) форма представления уравнений реакций между электролитами в водных растворах.
В ионно-молекулярных уравнениях реакций вещества малорастворимые, малодиссоциирован-ные и газообразные записываются в виде молекул, а сильные электролиты — в виде ионов, на которые они диссоциируют. Например, при взаимодействии растворов хлорида меди (II) и гидроксида натрия образуется осадок гидроксида меди (II): CuCl2 + 2NaOH = Cu(OH)2| + 2NaCl.
- В ионно-молекулярном виде уравнение этой реакции записывается следующим образом: Cu2+ + 2С1″ + 2Na+ + 20НГ = Cu(OH)2i + 2Na+ + 2СГ. Концентрации ионов натрия и хлора в процессе реакции остаются неизменными, поэтому из уравнения реакции их можно исключить. Поскольку реакции между ионами в растворе представляют собой пример химического равновесия, к ним применим принцип смещения равновесия Jle Шателье.
- В соответствии с этим принципом равновесие может сместиться, если какое-либо вещество будет удаляться из сферы реакции по мере ее протекания. Удаление вещества может быть осуществлено в трех случаях: 1) образование малорастворимого осадка; 2) выделение газообразного вещества; 3) образование малодиссоциированного соединения.
| При взаимодействии раствора |
(NH4)2S с соляной кислотой образуется газообразный сероводород и равновесие реакции смещается вправо: (NH4)2S + 2НС1 — 2NH4C1 + H2ST, 2NH4+ + S2″ + 2H4″ + 2СГ = 2NH4+ + 2СГ + H2Sf или 2H+ + S2″ = H2Sf.
Возможно вам будут полезны данные страницы:
Примером реакции, равновесие которой смещено в сторону образования малодиссоциированного соединения, может служить взаимодействие между растворами азотной кислоты и гидроксида натрия: HN03 + NaOH — NaN03 + Н20, Н+ + N03″ + Na+ + ОН» = Na+ + NO3- + Н20 или Н+ + ОН» — Н20. Реакция с образованием малорастворимого соединения была рассмотрена выше.
— S02t + H20. А при взаимодействии раствора гидроксида бария с серной кислотой одновременно образуются и осадок, и слабый электролит: Ва(ОН)2 + H2S04 = BaS04i + 2Н20, ‘ Ва2+ + 20Н» + 2Н* + S042’ » BaS04i + 2Н20. Некоторые реакции протекают с образованием двух труднорастворимых веществ: CuS04 + BaS = BaS04| + CuSj, Cu2+ + S042″ + Ba2* + S2″ = BaS04l + CuSi.
В ряде обменных процессов малодиссоциированные или труднорастворимые соединения находятся как среди исходных, так и конечных продуктов реакции: nh4oh + н+ + С1- ?± nh4+ + сг + н2о. Вследствие образования труднорастворимых соединений в отдельных случаях возможно вытеснение сильной кислоты из соединений слабой, например: Си24″ + 2СГ + H2S « CuSJ + 2Н* + 2СГ, Cu2+ + H2S-CuSi +2Н+. Таким образом, рассмотренные выше примеры подтверждают общую закономерность: все реакции обмена в растворах электролитов протекают в сторону уменьшения числа свободных ионов.
Присылайте задания в любое время дня и ночи в ➔
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.




























